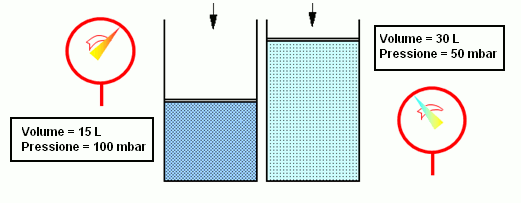
- La Legge di Boyle-Mariotte afferma che quando il volume di un gas diminuisce (ad esempio, sotto l’azione di un pistone), la pressione aumenta della stessa quantità, se la temperatura non cambia. Quindi il prodotto tra pressione e volume è uguale ad una costante: pV=cost e T=cost.
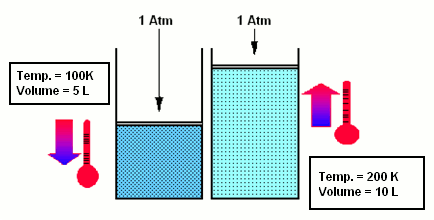
- La Legge di Charles afferma che, se la pressione è mantenuta costante, il volume del gas aumenta con il crescere della temperatura: V=V0 (1+atT) e p=cost.
- La Legge di Gay-Lussac afferma che, se il volume rimane costante, la pressione aumenta all’aumentare della temperatura secondo una relazione lineare. Il rapporto tra la variazione della pressione e quella della temperatura è uguale ad una costante: p=p0 (1+btT) e V=cost.












