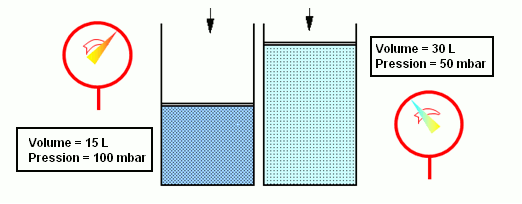
- Selon la loi de Boyle-Mariotte, lorsque le volume d’un gaz diminue (par exemple, sous l’action d’un piston), la pression augmente de la même quantité, si la température ne change pas. Le produit entre pression et volume est donc égal à une constante : pV=constante et T=constante
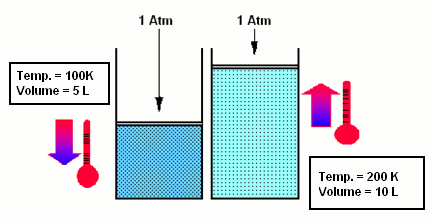
- Selon la loi de Charles, si la pression est maintenue à une valeur constante, le volume du gaz augmente lorsque la température augmente : V=V0 (1+atT) et p=constante.
- Selon la loi de Gay-Lussac, si le volume demeure constant, la pression augmente en fonction de l’augmentation de température selon une fonction linéaire. Le rapport entre la variation de la pression et la variation de la température est égal à une constante : p=p0 (1+btT) et V=constante.












